
Lo hizo ante el juez Alvin Hellerstein, luego de la lectura de los cargos por narcotráfico y terrorismo.


Tanto Pfizer-BioNTech como Moderna presentaron solicitudes en el ente regulador norteamericano por refuerzos contra estas variantes. Qué evaluarán para su aval y por qué
EL MUNDO28 de agosto de 2022



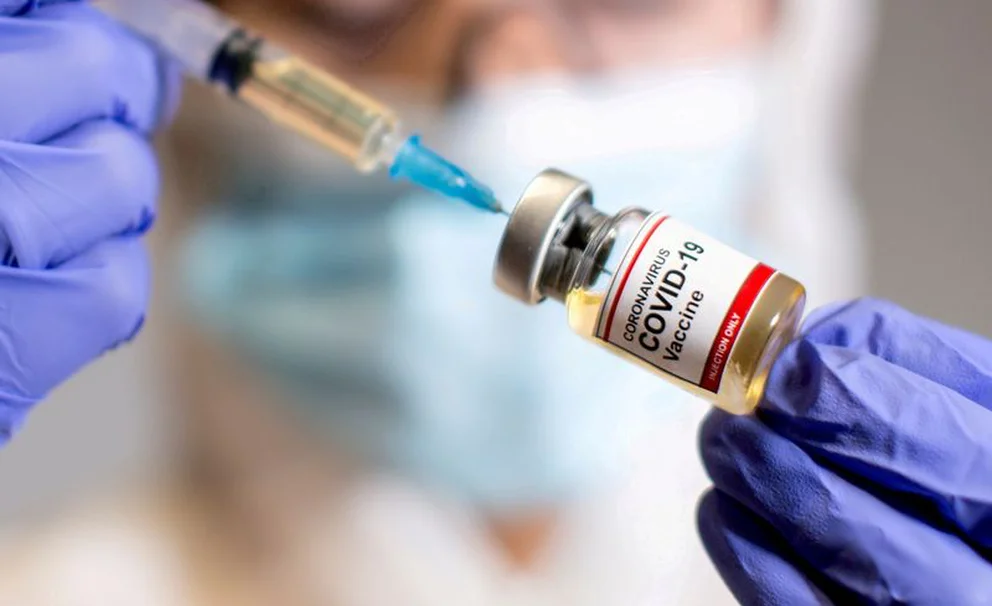


Desde que surgió el SARS-CoV-2, comenzó la carrera por alcanzar una vacuna que le ponga fin a la pandemia. Sin embargo, el virus mutó más rápido que las inmunizaciones, con lo cual se evidenció la necesidad de desarrollar dosis que pudieran combatir las nuevas variantes. Ahora, con la llegada de la versiones más contagiosas de Ómicron, la BA.4 y BA.5, tanto Pfizer-BioNTech como Moderna presentaron solicitudes para que la Administración de Drogas y Alimentos de los EEUU (FDA, por sus siglas en inglés) apruebe estas “nuevas versiones”. Aunque, según señalaron, solo se analizaron en animales.


Expertos a favor y en contra se desplegaron a ambos lados de esta posibilidad. Algunos argumentan que estas vacunas ya evidenciaron su seguridad y eficacia en humanos, por lo cual solo resta evaluar su comportamiento ante BA.4 y BA.5, las cuales dominan el globo y se muestran como las responsables de una nueva ola de casos a medida que el hemisferio norte ingresa en el invierno. Otros advierten la necesidad de completar estos ensayos clínicos, aunque sea en grupos reducidos.
Vale destacar que, según los Centros para el Control y la Prevención de Enfermedades (CDC, por sus siglas en inglés), la variante BA.5 de Ómicron es la responsable de casi el 89% de los casos, mientras que la BA.4 representa el 3,6% y la BA.4.6 el 7,%.
En la Argentina, según el último reporte de variantes emitido por el Ministerio de Salud en el Boletín epidemiológico, en las últimas semanas “la proporción de BA.4 aumenta de 9,2% a 13,6% (y a 15,5% si se consideran solo las muestras con identificación de linaje), BA.5 se incrementa de 8,5% a 14,8% (y a 16,9% si se consideran solo las muestras con identificación de linaje), Ómicron compatible con BA.4/BA.5 aumenta de 10% a 20,9% (y a 23,9% si se consideran solo las muestras con identificación de linaje)”.
“Es una cuestión de tiempo. La BA.5 se iba a terminar imponiendo. Estamos viviendo casi una inmunidad de rebaño. Más del 80% de la población ya se contagió y un buen grupo tiene recontagios. También más del 90% ya se dio el primer esquema de vacuna con dos dosis y más del 60% tiene una tercera o cuarta. Ese combo llamado inmunidad híbrida nos está protegiendo para que no tengamos una explosión de BA.5″, precisó a Infobae el médico clínico Luis Cámera.
Cronología: cómo se gestaron las nuevas vacunas contra BA.4 y BA.5 de Ómicron
El doctor Ashish Jha, coordinador de respuesta al COVID-19 de la Casa Blanca, se encuentra a la espera de que este nuevo refuerzo, específico contra las variantes más contagiosas de Ómicron, esté disponible desde mediados de septiembre, si es que la FDA y los CDC lo autorizan y recomienda, según consigna Time.
Es que desde finales de agosto, tanto Pfizer-BioNTech como Moderna, fabricantes de vacunas con plataforma de ARN mensajero, presentaron solicitudes para que sus nuevos refuerzos sean avalados por los entes reguladores norteamericanos. Sin embargo, estos datos suministrados son de eficacia y seguridad en animales. Es decir que aún no fueron probadas en humanos. Con lo cual, el proceso regulatorio y de revisión aún no se habría completado.
En junio, ambas empresas ya habían desarrollado una dosis contra la BA.1 de Ómicron. En ese mismo momento, un panel de expertos en vacunas independientes de la FDA se había expresado a favor de cambiar estas inmunizaciones hacia unas dirigidas contra las variantes que estaban dominando la escena norteamericana. Con lo cual no era solamente esta variante, sino también contra BA.4 y BA.5, principales responsables de los contagios. Por este motivo, les solicitaron a ambos fabricantes que generaran una inmunización que incluya estos sublinajes.
En meses lograron obtener una dosis que enfrentara a estas variantes, aunque al presentar los datos sobre seguridad y eficacia solo contaban con los efectuados en animales. Los estudios en humanos ya están planificados, de hecho Moderna ya lo inició, aunque de alcanzar la aprobación de la FDA se concretarían mientras estas inmunizaciones son aplicadas en el público en general.
Voces a favor y en contra: qué argumentan los expertos
Uno de los expertos que se mostró en contra de esta aprobación fue el doctor Paul Offit, miembro del comité asesor, quien afirmó sentirse “incómodo” ante esta situación, incluso ante la versión para BA.1. Según afirmó, los niveles de anticuerpos generados por la inmunización fueron decepcionantes. “Mostraron que los títulos de anticuerpos neutralizantes eran entre 1,5 y dos veces mayores contra Ómicron que los niveles inducidos por un refuerzo de la vacuna ancestral”, aseguró en diálogo con Time.
“Me gustaría ver evidencia clara de un aumento dramático en los anticuerpos neutralizantes, más dramático que lo que vimos contra BA.1, antes de lanzar un nuevo producto. Se nos debe al menos eso”, argumentó. Es más, el experto señalo que para controlar su efectividad y seguridad se puede concretar un pequeño ensayo, con unos 100 voluntarios. “Puedes estimular a las personas y medir sus anticuerpos neutralizantes dos semanas después”, explicó al evaluar las expectativas sobre esta nueva vacuna y agregó: “Francamente, me pongo un poco nervioso cuando escucho que este [refuerzo] va a ser milagroso”.
Del otro lado, el doctor Ofer Levy, director del programa de vacunas de precisión en el Boston Children’s Hospital y también miembro del comité asesor de vacunas de la FDA, se basó en el hecho de que estas inmunizaciones ya fueron aplicadas y evidenciaron su seguridad y eficacia en millones de personas en todo el planeta. Con lo cual, argumentó, estos aspectos ya fueron avalados y “no requiere las mismas pruebas exhaustivas que requería la inyección original”
“La totalidad de la evidencia es relevante aquí”, afirmó Levy. Al tiempo que destacó que “estamos en una situación en la que debemos cambiar a medida que surgen variantes, y si tratamos de ser demasiado rígidos en nuestro enfoque, siempre nos quedaremos atrás y no brindaremos a la población una protección óptima”. Incluso, señaló que, aunque los datos actuales provengan de animales, avalar estos refuerzos es una cuestión de “apuestas de cobertura” razonable. “Creo que es la decisión correcta”, añadió.
Reino Unido: el primer país en avalar los refuerzos contra las variantes de Ómicron
A finales de agosto, el Reino Unido se convirtió en el primer país en avalar estos refuerzos contra las variantes más contagiosas de Ómicron, aunque fue solo ante la BA.1. La nueva versión de la vacuna contra el covonavirus fue la desarrollada por el laboratorio Moderna y suma a la variante BA.1. Se trata de dosis bivalentes, las cuales están destinadas tanto al virus original del COVID-19, que se detectó en 2019 en Wuhan, China, como a esta versión de Ómicron.
Luego de que las autoridades sanitarias británicas avalaran estas nuevas dosis, Steve Barclay, secretario de Salud británico, afirmó que “las vacunas siguen siendo nuestra mejor defensa contra el coronavirus, y esta vacuna segura y eficaz ampliará la inmunidad y mejorará potencialmente la protección contra las nuevas variantes a medida que aprendamos a vivir con este virus”.
La médica patóloga pediátrica argentina Marta Cohen explicó que si bien la nueva vacuna fue rediseñada para combatir a Ómicron BA.1, que fue el primer sublinaje de la variante identificado, el laboratorio Moderna también “la ha probado con los sublinajes BA.4 y la BA.5, que es la que circula actualmente en el mundo y han visto que obtiene buenos resultados”. “No ha habido complicaciones serias”, agregó Cohen en un video compartido en sus redes sociales.
La experta argentina remarcó que, la aprobación británica se dio en el marco de una autorización de emergencia en el curso de la pandemia y que seguirá controlándose si hay algún tipo de complicación. “Pero aseguran que la eficacia permitiría armarnos, y esa es la palabra que utilizan, usar una armadura contra el virus que permitiría recibir una vacuna anualmente y no cada tan pocos meses como ocurre ahora”, señaló y concluyó: “Esperamos que esta vacuna sea administrada junto con la vacuna de la gripe, a partir del mes de septiembre, en el Reino Unido, que es cuando comienza el plan de vacunación (para el otoño boreal)”.
FUENTE: Infobae.





Lo hizo ante el juez Alvin Hellerstein, luego de la lectura de los cargos por narcotráfico y terrorismo.

El presidente de los Estados Unidos, Donald Trump, aseguró que tras la captura de Maduro y los ataques a Venezuela, su gobierno administrará ese país y que los representantes designados por él para hacerlo son Marco Rubio y Pete Hegseth. Los detalles

El presidente de Estados Unidos informó que su país llevó a cabo un “ataque a gran escala”.
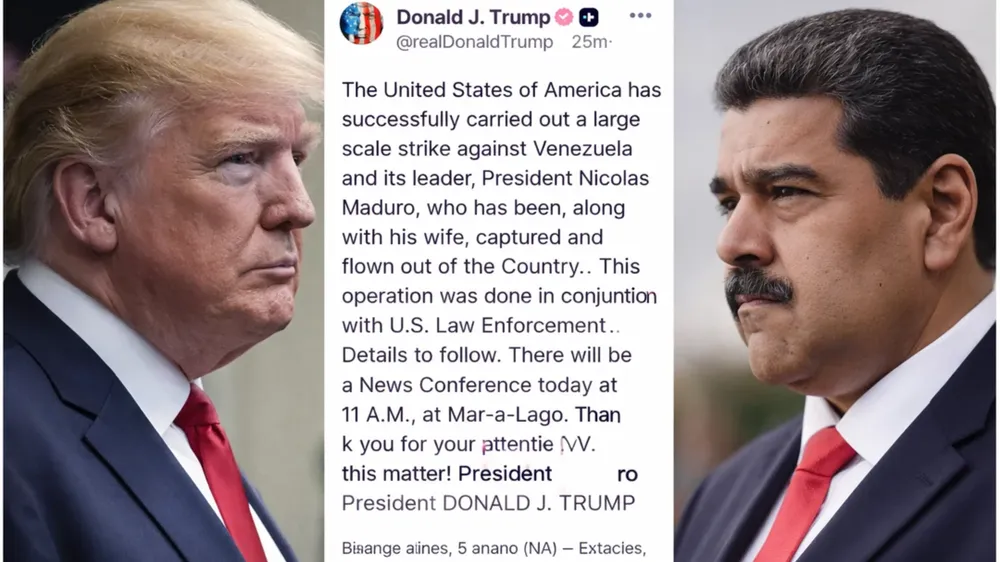
El presidente norteamericano dijo que Maduro y su esposa fueron “trasladados fuera del país”

La fiscalía investiga la negligencia en un bar de la exclusiva estación de esquí; el siniestro dejó 119 heridos.

Un avance histórico en la lucha contra el dengue: La Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil aprobó la Butantan-DV, la primera vacuna de una sola dosis contra la enfermedad. Desarrollada por el Instituto Butantan, estará disponible para personas de 12 a 59 años en el Programa Nacional de Inmunizaciones a partir de 2026.



El presidente de los Estados Unidos, Donald Trump, aseguró que tras la captura de Maduro y los ataques a Venezuela, su gobierno administrará ese país y que los representantes designados por él para hacerlo son Marco Rubio y Pete Hegseth. Los detalles

El mandatario venezolano y su esposa, Cilia Flores, comparecen ante un tribunal federal acusados de liderar una estructura ligada al narcotráfico y otros delitos graves.

La Justicia norteamericana incluyó a su esposa y su hijo en la acusación por narcotráfico y alianzas con grupos armados.

El tradicional festival se realizará del 9 al 11 de enero con entrada libre y gratuita. Habrá música, danza, actividades criollas y más de cinco millones de pesos en premios en el Desafío de Tropillas.

Brigadistas de Parques Nacionales y del Consejo Agrario Provincial trabajan desde temprano en el cerro Huemul. Está en camino un avión hidrante y continúa el operativo preventivo en la zona norte del área





